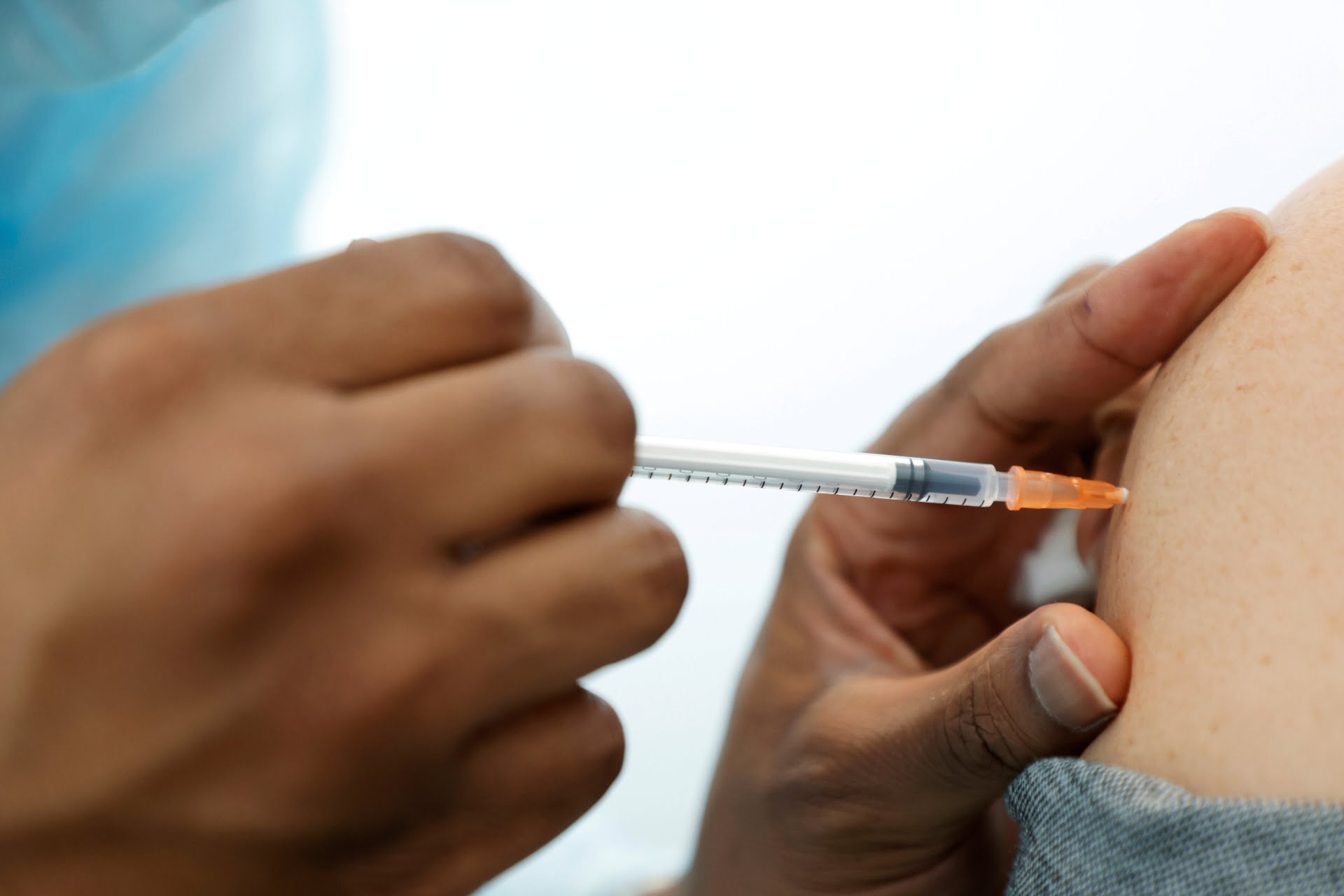
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou, nesta terça-feira (6), testes clínicos da vacina da Sanofi Pasteur contra a Covid-19 no Brasil. É o oitavo ensaio de vacina aprovado pela agência brasileira.
Os testes vão reunir 150 voluntários com no mínimo 18 anos de idade e serão conduzidos nos estados da Bahia, de Minas Gerais, do Mato Grosso do Sul e do Rio de Janeiro.
O ensaio aprovado no Brasil é de fase 1/2 e vai testar três diferentes dosagens da vacina para definir a dose ideal antes de prosseguir para um estudo de fase 3, última etapa. Serão duas doses, administradas com intervalo de 21 dias.
A Anvisa não informou a data de início dos testes. Um grupo de voluntários receberá uma substância inativa para comparação dos resultados (grupo placebo).
A nível global, a vacina será testada tambémnos EstadosUnidos, Honduras e Austrália. O desenvolvimento clínico está sendo patrocinado pela Sanofi, se aprovada, a candidata será fabricada pelas empresas Translate Bio, nos Estados Unidos, a Evonik Canada Inc., no Canadá, e a própria Sanofi, sediada na França e nos Estados Unidos.